咨询电话:010-67862040
非小细胞肺癌:
全球每年新发肺癌约 200万例(非小细胞肺癌约占85%),其中中国约占78.7万例,简言之,全世界每发生3例肺癌,就有1例在中国。1-3 MET ex14 skipping(MET外显子14跳读突变)是公认的致癌驱动因素,在新发肺癌中约占3~4%,在亚裔肺癌中约为5%,且MET ex14 跳读突变与其它已知的驱动基因相互排斥,多见于女性、老年患者、非吸烟者、肺肉瘤样癌,预后差。4-6
2020年5月6日,FDA加速批准诺华口服MET抑制剂 Tabrecta(capmatinib,卡马替尼)上市,用于一线及先前接受过治疗局部晚期(未扩散)或转移性(已扩散)MET ex14 跳读突变的非小细胞肺癌(NSCLC)患者。7 这是FDA批准的首个,全球上市的第二个(此前,默克Tepotinib于2020年3月26日在日本获批)用于治疗NSCLC患者特异性MET ex14 跳读突变的MET抑制剂。
什么是 MET ex14跳读突变?
MET (Mesenchymal epithelial transition factor),即间质上皮细胞转化因子,位于7号染色体,包括21个外显子和20个内含子,是一种多功能的跨膜酪氨酸激酶,是肝细胞生长因子HGF的受体,主要在上皮细胞中表达。
MET基因DNA水平第14外显子剪接区域位点(splice-sites)的突变导致MET第14外显子在mRNA水平出现部分或完全跳读缺失(ex14 skipping)。而MET ex14编码的近膜结构域能够参与MET蛋白的泛素化和降解,因此,MET 14外显子跳读将导致MET蛋白泛素化降解受阻,增加MET蛋白的稳定性,持续性表达,引起细胞内MET蛋白浓度升高,导致配体依赖的下游信号通路激活,从而促进肿瘤细胞生长与增殖(Fig 1)。8

Fig 1 MET正常剪接与异常剪接带来的不同结果
早检测早治疗获益会更高!
根据 GEOMETRY mono-1(NCT02414139)Ⅱ期临床试验中总体缓解率和缓解持续时间,FDA加速批准了capmatinib(卡马替尼)的上市,该适应症的持续批准可能要取决于验证性试验中对临床益处的验证和描述。9

Fig 2 GEOMETRY mono-1的疗效结果
研究结果显示,在28例初治患者中,ORR为 68%(其中4%为CR,64%为PR),DOR为 12.6个月;在69例经治患者中,ORR为 41%(41%为PR),DOR为 9.7个月,即无论患者先前是否曾接受过治疗,卡马替尼均能带来显著治疗效果。但是一线治疗的ORR(68% vs 41%)和 DOR(12.6个月 vs 9.7个月)却优于后线治疗的患者(Fig 2)。由此可见,NSCLC患者的基因检测很重要,早做基因检测,早发现早治疗,获益率会更高!
Digital PCR检测MET ex14 跳读:
数字PCR技术具有灵敏度高、特异性强、重复性好、可绝对定量的优点。APEXBIO依托Stilla的NaicaTM Crystal 微滴芯片数字PCR平台,开发了针对MET ex14跳读突变的数字PCR检测方法。(Fig 3)
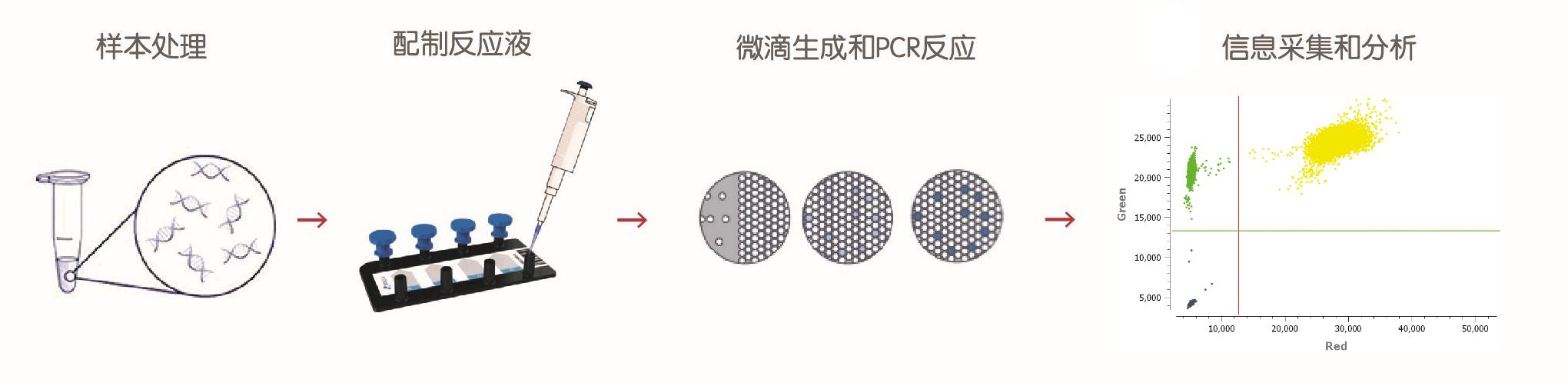
Fig 3 检测流程图
本检测方法中,于MET ex14跳读突变序列及其相邻序列设计探针(分别标记CY5和HEX)进行双重数字PCR反应(Fig 4),用配套的NaicaTM prism3微滴阅读分析系统采集PCR数据,最终检测结果可直观显示于2D图中(Fig 5)。

Fig 4 MET ex14 跳读引物探针设计示意图

Fig 5 Digital PCR检测MET ex14跳读突变2D图
在检测过程中全程封闭检测,不需转移液滴,可避免交叉污染,方便、准确、灵敏,为用户提供快速、精准的科研检测服务。对于其它基因、位点,我们也可提供个性化的数字PCR定制服务,包括实验设计、样本处理与纯化、引物探针设计与合成、实验优化、数字PCR检测以及数据分析等。
试剂盒信息:
MET ex14 skipping数字PCR检测试剂盒 (Apexbio, Cat No./ID: AK2001101)
参考资料:
1. World Health Organization. Cancer Fact Sheet, 2018.
2. American Cancer Society. Key Statistics for Lung Cancer.
3. 2015年中国恶性肿瘤流行情况分析,中华肿瘤杂志,2019年第41卷第1期
4. Sadiq AA, et al. Journal of Clinical Oncology. 2013;31:1089-1096.
5. Smyth EC, et al. Onco Targets and Therapy. 2014;7:1001-1014.
6. Salgia R. Molecular Cancer Therapeutics. 2017;16(4):555-565.
7.https://www.fda.gov/news-events/press-announcements/fda-approves-first-targeted-therapy-treat-aggressive-form-lung-cancer
8.Drilon Alexander, et al. .J Thorac Oncol, 2017, 12: 15-26.

